
Back Polêre molekule Afrikaans قطبية كيميائية Arabic Хімічная палярнасць Byelorussian Polaritat química Catalan Polaridad sa usa ka Kimikal CEB Polarität (Chemie) German Χημική πολικότητα Greek Chemical polarity English Polaridad (química) Spanish Molekuli polaarsus Estonian
 For alternative betydninger, se Polaritet.
For alternative betydninger, se Polaritet.
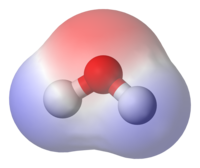
I kemi refererer polaritet til en ladningsforskydelse inden for et molekyle, hvormed én eller flere dele af molekylet bliver en anelse negativt og resten positivt. Denne polarisering skyldes forskel i elektronegativiteten mellem de forskellige komponenter af molekylet samt asymmetrien i strukturen.
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search